Olá pessoal do 9 ano metodista , aqui está o material dos modelos atômicos com seus desenhos um grande abraço a todos.
o endereço eletronico dos modelos usados nas simulações em aula é este aqui
http://phet.colorado.edu/en/simulation/hydrogen-atom
OS PRIMEIROS MODELOS ATÔMICOS
Alguns filosófo da Grécia Antiga já admitiam que toda e qualquer matéria seria formada por minúsculas partículas indivisíveis, que foram denominadas átomos (a palavra átomo, em grego, significa indivisível).
No entanto, foi somente em 1803 que o cientista inglês John Dalton, com base em inúmeras experiências, conseguiu provar cientificamente a idéia de átomo. Surgia então a teoria atômica clássica da matéria. Segundo essa teoria, quando olhamos, por exemplo, para um grãozinho de ferro, devemos imaginá-lo como sendo formado por um aglomerado de um número enorme de átomos. Os principais postulados da Teoria Atômica de Dalton são:
- a matéria é formada por partículas extremamente pequenas chamadas átomos;
- os átomos são esferas maciças, indestrutíveis e intransformáveis;
- átomos que apresentam mesmas propriedades (tamanho, massa e forma) constituem um elemento químico;
- átomos de elementos diferentes possuem propriedades diferentes;
- os átomos podem se unir entre si formando "átomos compostos";
- uma reação química nada mais é do que a união e separação de átomos.
MODELO ATÔMICO DE THOMSON
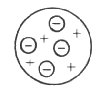
Em 1903, o cientista inglês Joseph J. Thomson, baseado em experiências realizadas com gases e que mostraram que a matéria era formada por cargas elétricas positivas e negativas, modificou o modelo atômico de Dalton. Segundo Thomson, o átomo seria uma esfera maciça e positiva com as cargas negativas distribuídas, ao acaso, na esfera. A quantidade de cargas positivas e negativas seriam iguais e dessa forma o átomo seria eletricamente neutro. O modelo proposto por Thomson ficou conhecido como "pudim com passas".
MODELO ATÔMICO DE
RUTHERFORD
Em 1911, o
cientista neozelandês Ernest Rutherford, utilizando os fenômenos radiativos no
estudo da estrutura atômica, descobriu que o átomo não seria uma esfera maciça,
mas sim formada por uma região central, chamada núcleo atômico, e uma região
externa ao núcleo, chamada eletrosfera. No núcleo atômico estariam as partículas
positivas, os prótons, e na eletrosfera as partículas negativas, os
elétrons.
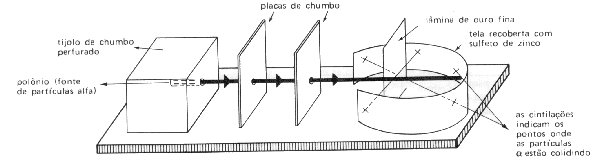
Para chegar a
essas conclusões Rutherford e seus colaboradores bombardearam lâminas de ouro
com partículas a (2 prótons e 2 nêutrons) utilizando a aparelhagem esquematizada
acima.
Rutherford
observou que a grande maioria das partículas atravessava normalmente a lâmina de
ouro que apresentava aproximadamente 10-5 cm de espessura. Outras
partículas sofriam pequenos desvios e outras, em número muito pequeno, batiam na
lâmina e voltavam. O caminho seguido pelas partículas a podia ser detectado
devido ?s cintilações que elas provocavam no anteparo de sulfeto de
zinco.
Comparando o
número de partículas a lançadas com o número de partículas a que sofriam
desvios, Rutherford calculou que o raio do átomo deveria ser 10.000 a 100.000
vezes maior do que o raio do núcleo, ou seja, o átomo seria formado por espaços
vazios. Por esses espaços
vazios a grande maioria das partículas a atravessava a lâmina de
ouro.
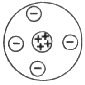 Os desvios sofridos pelas
partículas a eram devidos às repulsões elétricas entre o núcleo (positivo) e as
partículas a, também positivas, que a ele se dirigiam. O modelo de Rutherford
(figura ao lado) ficou conhecido como "modelo planetário".
Os desvios sofridos pelas
partículas a eram devidos às repulsões elétricas entre o núcleo (positivo) e as
partículas a, também positivas, que a ele se dirigiam. O modelo de Rutherford
(figura ao lado) ficou conhecido como "modelo planetário".
observação importante
A quantidade atômica de prótons e elétrons
presentes num átomo é a mesma, o que faz com que ele seja eletricamente neutro
repare que a fisica não se separa da fisica
Em 1913, o físico
dinamarquês Niels Bohr, ao estudar espectros de emissão de certas substâncias,
modificou o modelo de Rutherford. No inicio do século XX era fato conhecido que
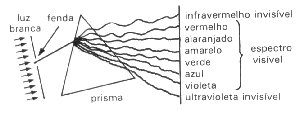
a luz branca (luz solar, por exemplo) podia ser decomposta em diversas cores.
Isso é conseguido fazendo com que a luz passe por um prisma. No caso da
decomposição da luz solar obtém-se um espectro chamado espectro continuo. Este é
formado por ondas eletromagnéticas visíveis e invisíveis (radiação ultravioleta
e infravermelho). Na parte visível desse espectro não ocorre distinção entre as
diferentes cores, mas uma gradual passagem de uma para outra. O arco-íris é um
exemplo de espectro contínuo onde a luz solar é decomposta pelas gotas de água
presentes na atmosfera. Como a cada onda eletromagnética está associada certa
quantidade de energia, a decomposição da luz branca produz ondas
eletromagnéticas com toda e qualquer quantidade de energia.
No entanto, se a
luz que atravessar o prisma for de uma substância como hidrogênio, sódio, neônio
etc. será obtido um espectro descontínuo. Este é caracterizado por apresentar
linhas coloridas separadas. Em outras palavras, somente alguns tipos de
radiações luminosas são emitidas, isto é, somente radiações com valores
determinados de energia são emitidas.
Baseado nessas
observações experimentais, Bohr elaborou um novo modelo atômico cujos postulados
são:
- na eletrosfera os elétrons não se encontram em qualquer posição. Eles giram ao redor do núcleo em órbitas fixas e com energia definida. As órbitas são chamadas camadas eletrônicas, representadas pelas letras K, L, M, N, O, P e Q a partir do núcleo, ou níveis de energia representados pelos números 1, 2, 3, 4...;
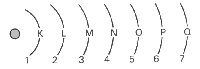
- os elétrons ao se movimentarem numa camada eletrônica não absorvem nem emitem energia;
- os elétrons de um átomo tendem a ocupar as camadas eletrônicas mais próximas do núcleo, isto é, as que apresentam menor quantidade de energia;
- um átomo está no estado fundamental quando seus elétrons ocupam as camadas menos energéticas;
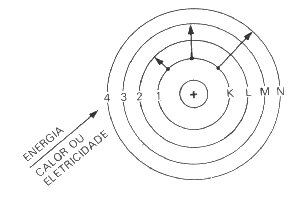
- quando um átomo recebe energia (térmica ou elétrica), o elétron pode saltar para uma camada mais externa (mais energética). Nessas condições o átomo se torna instável. Dizemos que o átomo se encontra num estado excitado;
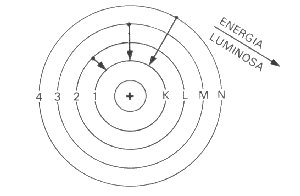
- os elétrons de um átomo excitado tendem a voltar para as camadas de origem. Quando isso ocorre, ele devolve, sob a forma de onda eletromagnética, a energia que foi recebida na forma de calor ou eletricidade.
Esses postulados
permitem explicar a existência dos espectros de emissão descontínuos: como o
elétron só pode ocupar determinadas órbitas, as transições eletrônicas (ida e
volta do elétron) ocorrem em número restrito, o que produz somente alguns tipos
de radiação eletromagnética e não todas como no espectro contínuo.
Modelo atômico de
Bohr foi elaborado para o átomo de hidrogênio, mas aplica-se com boa aproximação
a todos os outros átomos.
Nenhum comentário:
Postar um comentário